Hauptindikatoren 1 - 10
| Nummer | Hauptindikatoren 1-10 |
| I | Tägliche multiprofessionelle und interdisziplinäre klinische Visite mit Dokumentation von Tageszielen |
| II | Management von Sedierung, Analgesie und Delir |
| III | Patientenadaptierte Beatmung (bei schwerem Lungenversagen) |
| IV | Frühzeitige Entwöhnung von einer invasiven Beatmung (Weaning) |
| V | Überwachung der Maßnahmen zur Infektionsprävention |
| VI | Maßnahmen zum Infektionsmanagement |
| VII | Patientenadaptierte klinische Ernährung |
| VIII | Strukturierte Kommunikation mit Patienten und Angehörigen |
| IX | Frühmobilisation |
| X | Personalbesetzung und Strukturvoraussetzungen einer Intensivstation |
![]() Hier können Sie alle Hauptindikatoren mit Literaturhinweisen als PDF herunterladen
Hier können Sie alle Hauptindikatoren mit Literaturhinweisen als PDF herunterladen

Tägliche multiprofessionelle und interdisziplinäre Visite mit Dokumentation von Tageszielen
|
Größenordnung |
Risiko und Effektivität |
|
Art des Indikators |
Prozess |
|
Begründung |
Die tägliche multiprofessionelle und interdisziplinäre Visite verbessert die Kommunikation der an der Behandlung beteiligten Professionen auf einer Intensivstation. Von besonderer Bedeutung ist dabei die schriftliche Dokumentation der Tagesziele für jeden Patienten. Die Festlegung von täglichen (kurzfristigen) und längerfristigen Zielen soll zur effektiveren Umsetzung geplanter Maßnahmen unter Berücksichtigung der Therapieziele führen und somit die Behandlungsqualität verbessern. An der Schnittstelle “Übergabe und Visite” besteht durch mangelhaft strukturierte Durchführung und Dokumentation der Patientenübergabe das Risiko von Informationsverlusten und dadurch Qualitätsverlusten. |
|
PICO |
Die Durchführung einer täglichen, multiprofessionellen und interdisziplinären Visite mit Dokumentation von Tageszielen verbessert die Kommunikation unter den beteiligten Personen und verbessert das Behandlungsergebnis im Vergleich zu einer unstrukturierten Visite |
|
Qualitätsziel |
Durchdringung des täglichen Ablaufs auf einer Intensivstation mit vorgegebenen Tageszielen und Durchführung einer multidisziplinären Visite. |
|
Prozessqualität Zähler |
Tägliche Visiten mit Tageszielfestlegung, die nachvollziehbar dokumentiert sind |
|
Nenner |
Alle Behandlungstage eines Patienten auf der Intensivstation |
|
Erklärung der Terminologie |
Visite: Tägliche interprofessionelle und – je nach Behandlungsspektrum der Intensivstation – auch interdisziplinäre Fallbesprechung unter Anwesenheit mindestens eines Entscheidungsträgers (Leiter der Intensivstation bzw. vertretender Oberarzt/FA mit ZB Intensivmedizin). Visiten auf Intensivstationen sollen bettseitig allen beteiligten Professionen einen Informationsfluss im Kontext des klinischen Bildes der Patienten ermöglichen. Tagesziele: Die Festlegung der Tagesziele bei der Visite sollte unter Einbeziehung der beteiligten Professionen und Disziplinen indikationsbezogen erfolgen.
Dokumentation: Je mehr Professionen oder Disziplinen an der Behandlung des Patienten beteiligt sind, desto schwerer wird es, die Beteiligten synchron zu einer Visite zu vereinen. Daher gewinnen schriftliche Festlegungen an Bedeutung, um den Informationsfluss interprofessionell und integrativ zu garantieren. Änderungen bei den Zielfestlegungen werden durch die Verschriftlichung ebenfalls ermöglicht, weil zu diskutierende Punkte von den dokumentierten Beteiligten aufgegriffen werden können. |
|
Datenquelle |
Patientenakte, PDMS |
|
Richtwert |
90% korrekt dokumentierte Visiten |
|
Evidenzgrad |
Expertenkonsens |
|
QUALIFY |
Fakultative Bewertung |
|
Beteiligte |
R. Wildenauer, A. Brinkmann, A. Markewitz, M. Assenheimer |
|
Interessenkonflikte |
Siehe Anhang |
|
Literatur |
(1-11) |
|
Zusatzinformationen |
·Validierte Tagesziele/Items:
·TRIKK: 5 Leitfragen, welche während der Visite einfach abgearbeitet werden können - Leitfaden zur Berücksichtigung des Patientenwillens (Akronym):
|
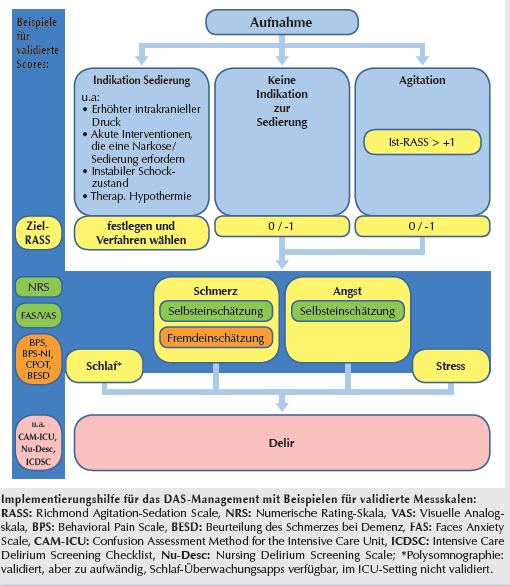
Management von Sedierung, Analgesie und Delir
|
Größenordnung |
Risiko und Effektivität |
|
Art des Indikators |
Struktur, Prozess |
|
Begründung |
Eine inadäquate Sedierung (Übersedierung oder Untersedierung), eine inadäquate Analgesie und ein unbehandeltes Delir verursachen eine Steigerung von Morbidität, Letalität sowie des Ressourcenverbrauchs. Ein multimodales Konzept zum Management von Analgesie, Sedierung und Delir soll als Standard auf jeder Intensivstation vorhanden sein. Die regelmäßige Überwachung von Sedierungstiefe und Analgesiequalität sowie Nutzung von Instrumenten zur Erkennung eines Delirs sind die Voraussetzung für die Umsetzung eines solchen Konzeptes.
Delir (z. B. Beurteilung der Prävalenz; wurde eine Therapie eingeleitet? Wenn ja, welche?) |
|
PICO |
Kann die regelmäßige, kontinuierliche Messung von Scorewerten zu den Bereichen Sedierung, Schmerz und Delir im Vergleich zur Nicht-Messung den Behandlungsprozess in diesen Dimensionen bei erwachsenen Intensivpatienten verbessern |
|
Qualitätsziel |
Es soll sichergestellt werden, dass die Überwachung von unangemessener Sedierung, unzureichender Schmerztherapie und das Erkennen eines Delirs zeitnah und kontinuierlich über den gesamten Behandlungsverlauf erfolgt |
|
Strukturqualität |
Ein Standard zum Management von Sedierung, Analgesie und Delir ist vorhanden |
|
Zähler |
Anzahl aller durchgeführten SCORE-Messungen |
|
Nenner |
Gesamtzahl vorgegebener Messungen bei allen intensivmedizinisch behandelten Patienten während des gesamten Behandlungszeitraums. |
|
Erklärung der Terminologie |
Der Einsatz validierter Sedierungs-, Analgesie- und Delirskalen wird in den klinischen Leitlinien empfohlen:
oder andere validierte Delir Scores. |
| Datenquelle |
Abfrage: Peer Review |
|
Richtwert |
|
|
Evidenzgrad |
Expertenkonsens |
|
QUALIFY |
Fakultative Bewertung |
|
Beteiligte |
O. Kumpf, P. Czorlich, S. Krotsetis |
|
Interessenkonflikte |
Analog zu den AWMF-COI Einträgen |
|
Literatur |
(12) |
| Weitere INformationen |
Algorithmus Scoring
Algorithmus aus Wolf A., et al. Anästh Intensivmed 2016;57:41-44) |
Patientenadaptierte Beatmung
(bei schwerem Lungenversagen)
|
Größenordnung |
Risiko und Effektivität |
|
Art des Indikators |
Struktur und Prozess |
|
Begründung |
Das schwere akute Lungenversagen (ARDS) erfordert an den individuellen Patienten angepasste Beatmungs- und Lagerungsstrategien mit dem Ziel, weitere pulmonale und systemische Schäden zu vermeiden und das Outcome zu verbessern. Weltweit erkennen Intensivmediziner ein ARDS oft spät oder gar nicht, und bisherige Behandlungsstandards werden auch deshalb nicht konsequent angewandt. Ein standardisiertes, abgestuftes Konzept zur Beatmungstherapie (Beatmungsstandard) des schweren akuten Lungenversagens kann das Überleben dieser verbessern und sollte daher auf jeder Intensivstation vorgehalten werden. Das Konzept sollte ein abgestuftes Vorgehen beschreiben, dass sich an den aktuellen S3-LL zur invasiven Beatmung und zur Lagerungstherapie des AWMF-Registers orientiert. Es sollte prozesshaft die unterschiedlichen Aspekte der Beatmungsoptimierung (z. B. Verfahren der PEEP-Optimierung, Begrenzung der tidalen Dehnung und des Driving Pressures (deltaP=VT/Compliance)) enthalten und adjunktive Therapien wie Bauchlagerung bis hin zur Einbeziehung eines ARDS-Zentrums berücksichtigen, sofern extrakorporale Lungenersatzverfahren nicht selbst durchgeführt werden. |
|
PICO |
Kann die Verwendung eines Beatmungsstandards im Vergleich zu einem Vorgehen ohne festgelegten Standard bei erwachsenen Patienten mit schwerem akuten Lungenversagen (ARDS) die Morbidität und Mortalität verringern? |
|
Qualitätsziel |
Der Indikator soll zur Verbesserung des Behandlungsergebnisses des schweren Lungenversagens beitragen, indem standardisierte, an den neuesten Erkenntnissen der EBM orientierte Behandlungsverfahren bei der Therapie des ARDS angewandt werden. Dabei steht die individualisierte Beatmungsstrategie im Vordergrund |
|
Strukturqualität |
Beatmungsstandard ist vorhanden: ja / nein |
|
Prozessqualität |
Anzahl der Patienten mit schweren Lungenversagen und Therapie nach leitlinienbasiertem Beatmungsstandard |
|
Nenner |
Alle maschinell beatmeten Patienten mit Lungenversagen |
|
Erklärung der Terminologie |
Das Ziel der patientenadaptierten Beatmung ist die Sicherstellung eines adäquaten (nicht unbedingt physiologischen) Gasaustausches unter Vermeidung sekundärer Lungenparenchymschäden und Verstärkung der systemischen Inflammation (Biotrauma). Adjunktive Maßnahmen wie Bauchlagerung können dies bei schwerem ARDS unterstützen. Bestandteile des Standards zur patientenadaptierten Therapie sollten eine Begrenzung des Tidalvolumens (VT 6-7ml/kg Idealgewicht), Limitierung des Plateaudrucks (30 cmH2O) sowie eine individualisierte PEEP-Einstellung beinhalten. Der Driving Pressure berücksichtigt neben dem VT auch die Compliance und ist damit besser zur Abschätzung der mechanischen Belastung durch Beatmung geeignet als VT alleine. DeltaP >14-15 cmH2O sind mit einer Übersterblichkeit assoziiert. Eine Individualisierung des PEEP kann sich pragmatisch am Ausmaß der Hypoxämie orientieren (z. B. PEEP-Tabelle). Weiterhin sollten patientenbezogene Faktoren (z. B. Lungenvorschädigung, Adipositas, Hämodynamik) berücksichtigt werden. Dies kann bettseitig erhobene Messdaten (z. B. Driving Pressure, transpulmonaler Druck, HZV) und bildgebende Diagnostik (z.B. Thorax-CT, Ultraschall, EIT) beinhalten. Rekrutierungsmanöver sollten nicht generell verwendet werden. Bei Patienten mit PaO2/FIO2<150mmHg wird eine Bauchlagerung empfohlen. Bei fehlenden Kontraindikationen (z.B. erhöhtem intrakraniellen Druck) sollte augmentierte Spontanatmung frühzeitig ermöglicht werden, da dies eine bessere basale Lungenbelüftung, weniger Analgo-Sedierung und eine verbesserte Hämodynamik ermöglicht. Muskelrelaxierung kann nicht (mehr) generell empfohlen werden. Für den Bedarfsfall sollte ein Verlegungsprozess in ein spezialisiertes Zentrum zur Behandlung des schweren Lungenversagens mit extrakorporalen Lungenersatzverfahren etabliert sein. |
|
Datenquelle |
Abfrage: Peer Review |
|
Richtwert |
|
|
Evidenzgrad |
Expertenkonsens |
|
QUALIFY |
Fakultative Bewertung |
|
Beteiligte |
P. Schürholz, H. Wrigge, B. Kruger, O. Kumpf |
|
Interessenkonflikte |
Siehe Anhang |
|
Literatur |
(13-21) |
| Weitere Informationen | entfällt |
Frühzeitige Entwöhnung von einer invasiven Beatmung (Weaning)
|
Größenordnung |
Risiko und Effektivität |
|
Art des Indikators |
Struktur, Prozess und Outcome |
|
Begründung |
Eine invasive Beatmung ist mit dem Risiko von Komplikationen (z.B. beatmungsassoziierten Pneumonie (VAP), beatmungsassoziierter Lungenschädigung (VILI), Delir, Atrophie der Atemmuskulatur) verbunden. Therapeutisches Ziel ist es daher, in Abhängigkeit vom Krankheitszustand durch frühzeitige Entwöhnung von einer invasiven Beatmung eine möglichst kurze Beatmungsdauer zu erreichen. In Abhängigkeit von der Art und Schwere der Erkrankung sollte auch geprüft werden, ob durch die sachgemäße Anwendung einer nicht-invasiven Beatmung (NIV) oder durch die Applikation von Sauerstoff über Highflow-Systeme (high flow nasal canula, HFNC) eine invasive Beatmung ganz vermieden oder eine Reintubation nach primär erfolgreicher Extubation verhindert werden kann. |
|
PICO |
Verkürzt ein strukturiertes Weaning anhand eines Protokolls die Beatmungsdauer und vermindert die Zahl der Patienten mit erfolglosem prolongierten Weaning im Vergleich zu einem Weaning ohne Protokoll |
|
Qualitätsziel |
Möglichst niedrige Anzahl erfolgloser Beatmungsentwöhnungen |
|
Strukturqualität |
Vorliegen eines Leitlinien-basierten Konzeptes (SOP) für das Weaning, insbesondere auch für das prolongierte Weaning und einer strukturierten Weaning-Dokumentation in der Krankenakte |
|
Prozessqualität |
Anzahl der invasiv beatmeten Patienten, bei denen die Entwöhnbarkeit evaluiert und/oder ein Weaningversuch dokumentiert wurde |
|
Nenner |
Alle invasiv beatmeten Patienten |
|
Ergebnisqualität |
Anzahl der Patienten, die nach erfolglosem Weaning in eine invasive außerklinische Beatmung überführt wurden (Fakultative Erhebung) |
|
Erklärung der Terminologie |
Struktur- und Prozessmerkmale Tägliche Überprüfung der Voraussetzungen für ein Weaning und einen Spontanatmungsversuch, möglichst unter Einsatz eines standardisierten Weaning-Protokolls. Hier besteht auch ein enger Zusammenhang mit dem QI II, der die tägliche Zielvorgabe der Sedierung und die Dokumentation der erhobenen Werte vorgibt. Ein leitlinien-basiertes Konzeptes (z. B. SOP) für das Weaning, insbesondere auch für das prolongierte Weaning, sollte durch ein interprofessionelles Behandlungsteam (Ärzte, Pflege, Physiotherapie, Atmungstherapie, Logopädie) umgesetzt werden. Eine nachvollziehbare Weaning-Dokumentation in der Krankenakte, inkl. der Durchführung und Dokumentation einer wöchentlichen Weaning-Besprechung ist notwendig und erleichtert auch die Umsetzung des neu geschaffenen Weaning-OPS |
|
Datenquelle |
Struktur: Standard/SOP Weaningkonzepte vorhanden |
|
Richtwert |
Struktur ja/ nein - ja 100% |
|
Evidenzgrad |
Expertenkonsens |
|
QUALIFY |
Fakultative Bewertung |
|
Beteiligte |
R. Riessen, H. Habermehl, O. Kumpf |
|
Interessenkonflikte |
Keine |
|
Literatur |
(15, 22, 23) |
|
Ergänzende Informationen |
Entfällt |
Überwachung der Maßnahmen zur Infektionsprävention
|
Größenordnung |
Risiko und Effektivität |
|
Art des Indikators |
Struktur, Prozess und Ergebnis |
|
Begründung |
Patienten der Intensivstation weisen im Krankenhaus ein deutlich erhöhtes Infektionsrisiko auf. Dies gewinnt mit zunehmendem Auftreten multiresistenter Erreger (MRE) immer mehr an Bedeutung. Im Rahmen des Infektionsschutzgesetzes tragen medizinische Einrichtungen eine hohe Verantwortung in der Vermeidung von Infektionen. 1. Strukturqualität: 2. Prozessqualität:
3. Ergebnisqualität
sind typische infektiologische Komplikationen der Intensivstation, für deren Prävention entsprechende Empfehlungen existieren. Die Überwachung der Häufigkeit wenigstens einer dieser Infektionen (Surveillance) bietet die Möglichkeit, Probleme im Hygiene-Management zu identifizieren und den Erfolg einer Qualitäts-verbessernden Maßnahme zu messen. Die Teilnahme an dem Modul ITS-KISS des Nationalen Referenzzentrums für Surveillance von nosokomialen Infektionen (NRZ) ist ein geeignetes Werkzeug, die Dokumentation der Ergebnisqualität zu unterstützen. |
|
PICO |
Kann durch die Anwendung eines Standards zur Prävention für nosokomiale Infektion und Infektionssurveillance im Vergleich zu einem Vorgehen ohne diese Maßnahmen die Häufigkeit von nosokomialen Infektionen verringert werden? |
|
Qualitätsziel |
Der Qualitätsindikator Infektionsprävention überwacht die Struktur, Prozess- und Ergebnisqualität als Maß für die Umsetzung der Leitlinien zur Infektionsprävention. Es soll sichergestellt werden, dass aktuelle Empfehlungen zur Infektionsprävention auf Intensivstationen umgesetzt werden. |
|
Strukturqualität |
SOPs für Infektionsprävention vorhanden |
|
Prozessqualität |
|
|
Zähler |
Anzahl der STOP ORDERS |
|
Nenner |
Anzahl invasiver Devices |
|
Zähler |
Händedesinfektionsmittelverbrauch in Liter |
|
Nenner |
1000 Patiententage |
|
Ergebnisqualität |
ITS-KISS des NRZ |
|
Zähler |
Anzahl der Infektionsereignisse per Device |
|
Nenner |
1000 Devicetage |
|
Erklärung der Terminologie |
Fünf Indikationen der Händedesinfektion:
Mögliche Maßnahmen zur VAP-Prophylaxe Zu diesem Zwecke werden in der Literatur verschieden Maßnahmen genannt, die entweder als Maßnahmenbündel (VAP Bundle) oder als Einzelmaßnahme zur Reduktion der Inzidenz von VAP beitragen können. Die Zusammensetzung der VAP Bundle unterscheidet sich in der Literatur, so dass es im in Anbetracht des positiven Outcome-relevanten Effektes der Bundle keine klare Zuordnung zu nur einer der genannten Maßnahmen geben kann. VAP Bundle als solche sind jedoch nachweißlich dazu geeignet, die Inzidenz von VAP zu reduzieren. Es wird empfohlen, mindestens drei Maßnahmen eines VAP Bundle in den Standards der Intensivstation hinterlegt zu haben, z.B.: Mundpflege und orale Dekontamination mit antiseptischen Lösungen (ODD), Vermeidung oraler Aspiration z.B. durch regelmäßige Cuffdruckmessungen, kontinuierliche subglottische Sekretabsaugung. Es gibt Hinweise, dass eine Chlorhexidin-haltige Mundhygiene die VAP-Häufigkeit reduziert, ohne allerdings den weiteren Verlauf (z.B. Beatmungsdauer, ITS-Liegezeit, Sterblichkeit) zu beeinflussen. Mögliche Nebenwirkungen sind nur unzureichend untersucht. Mögliche Maßnahmen zur CLABSI-Prophylaxe Es wird empfohlen, SOP für die Anlage und Pflege der intravasalen Katheter vorzuhalten und deren Anwendung zu schulen. Maßnahmen zur Anlage der Katheter sollten enthalten: Händedesinfektion vor Punktion, Angaben zur Wahl der Hautdesinfektion (z.B. Chlorhexidin-haltige Lösungen), Maximum Sterile Barrier Precaution (Sterile Handschuhe, steriler Kittel, Maske, ausreichend große sterile Abdeckung), Angaben zu Punktionstechniken (Vermeidung der V. femoralis als Punktionsort, Sonografie). Maßnahmen zur Pflege der Katheter sollten Angaben zur Desinfektion bei Benutzung des Katheters, Indikationen zur Nutzung (Vermeidung unnötiger Manipulationen) sowie Entfernung des Katheters und Pflege der Einstichstelle enthalten. Mögliche Maßnahmen zur CAUTI-Prophylaxe Es wird empfohlen, SOP für die Anlage und Pflege für Harnblasen-Katheter vorzuhalten und deren Anwendung zu schulen. Maßnahmen zur Anlage der Katheter sollten enthalten: Indikationsstellung und tägliche Überprüfung, Legen des Katheters unter aseptischen Bedingungen, Verwendung von sterilen und geschlossenen Harnableitungssystemen, Management des liegenden Katheters, Vorgaben zum Leeren des Beutels, Management bei Entfernung des Katheters. Mögliche Maßnahmen zur Prophylaxe von Infektionen von Liquordrainagen Es wird empfohlen, SOP für die Anlage und Pflege für Liquordrainagen vorzuhalten und deren Anwendung zu schulen. Möglichst Anlage der Liquordrainagen im OP. Maßnahmen zur Anlage der Drainagen sollten enthalten: Händedesinfektion vor Punktion, Angaben zur Wahl der Hautdesinfektion (z.B. Chlorhexidin-haltige Lösungen), Maximum Sterile Barrier Precaution (s.o.), alle 2-3 Tage routinemäßiges und bei entsprechender Klinik mikrobiologisches Liquor-Monitorring, tägl. Kontrolle (und Dokumentation) der Punktionsstelle. |
|
Datenquelle |
Abfrage: Peer Review |
|
Richtwert |
Struktur:
Prozess:
Ergebnis:
|
|
Evidenzgrad |
Expertenkonsens |
|
QUALIFY |
Fakultative Bewertung |
|
Beteiligte |
F. Bloos, A. Brinkmann, G. Wöbker, P. Czorlich |
|
Interessenkonflikte |
Siehe Anhang |
|
Literatur |
(24-31) |
|
Ergänzende Informationen |
entfällt |
Maßnahmen zum Infektionsmanagement
|
Größenordnung |
Risiko und Effektivität |
|
Art des Indikators |
Struktur, Prozess und Ergebnis |
|
Begründung |
Frühzeitige, adäquate und effektive Infektionsdiagnostik, antiinfektive Therapie und die effektive Vermeidung von Resistenzentwicklung und Kollateralschäden vor allem im gastrointestinalen Mikrobiom sind in Bezug auf das Management von Infektionen auf der Intensivstation von herausragender Bedeutung. Nach folgenden Grundsätzen soll gehandelt werden:
Für die Implementierung eines zuverlässigen und effektiven Infektionsmanagements ist eine interdisziplinäre und interprofessionelle Zusammenarbeit am besten in einem fest etablierten ABS-Team empfehlenswert. |
|
PICO |
Kann die Anwendung eines Standards und die Überwachung der angemessenen Anwendung von Leitlinien und Überwachung von Methoden der Erregerdiagnostik das Behandlungsergebnis bei Pateinten mit Sepsis verbessern im Vergleich zu einer nicht standardisierten und überwachten Diagnostik und Therapie. |
|
Qualitätsziel |
Durch frühzeitige, adäquate und effektive Infektionsdiagnostik, Fokuskontrolle und antiinfektive Therapie wird ein relevanter Beitrag zur Verbesserung des Outcomes (Sterblichkeit, Komplikationen und Behandlungsdauer) von kritisch kranken Patienten mit schweren Infektionen, Sepsis und septischem Schock geleistet. Rationaler, gezielter und reliabler Einsatz von antiinfektiven Substanzen leistet im Weiteren einen gewichtigen Beitrag zur Reduktion der Resistenzentwicklung und der Behandlungskosten. |
|
Strukturqualität |
SOP zum Infektionsmanagement vorhanden |
|
Prozessqualität Zähler |
Anzahl adäquate Antibiotikatherapien |
|
Nenner |
Alle intensivmedizinisch überwachten und behandelten Patienten mit DRG-Code. |
|
Prozessqualität Zähler |
Anzahl adäquater Dokumentation (Indikation, Fokus, voraussichtliche Therapiedauer, aktuelle LL) |
|
Nenner |
Alle intensivmedizinisch überwachten und behandelten Patienten mit DRG-Code. |
|
Ergebnisqualität Zähler |
Anzahl der abgenommenen Blutkulturen |
|
Nenner |
1000 Patiententage |
|
Erklärung der Terminologie |
Mit der Neuformulierung der Sepsis-Definition im Jahr 2016 wird der Fokus auf klinische Aspekte gelegt. Zusätzlich wird dem SOFA-Score eine wichtige Rolle in der Detektion der Sepsis zugedacht. Es wird empfohlen die Teilkomponenten des SOFA-Scores täglich bei allen Patienten mit relevantem Sepsisrisiko zu erfassen. Methoden zur Verbesserung der antiinfektiven Therapie im Umfeld der Intensivmedizin umfassen: Strukturqualität:
Prozessqualität:
Ergebnisqualität: Erfassung geeigneter Kennzahlen zur Bewertung der Effektivität der vorgegebenen Standards:
|
|
Datenquelle |
Abfrage Peer Review |
|
Richtwerte |
|
|
Evidenzgrad |
Expertenkonsens |
|
QUALIFY |
Fakultative Bewertung |
|
Beteiligte |
A. Brinkmann, F. Bloos, G. Wöbker |
|
Interessenkonflikte |
Siehe Anhang |
|
Literatur |
(25, 32-43) |
|
Ergänzende Informationen |
Nutzung von Dosis-Kalkulationstools zur Dosisfindung bei eingeschränkter Nierenfunktion Kalkulationstools: |
Patientenadaptierte Klinische Ernährung
|
Größenordnung |
Risiko und Effektivität |
|
Art des Indikators |
Struktur und Prozess |
|
Begründung
|
Bei fast allen Intensivpatienten ist eine zeitnahe klinische Ernährungstherapie erforderlich. Ursache hierfür kann z. B. eine Mangelernährung, starkes Übergewicht eine schwere metabolische Störung oder eine Substratverwertungsstörung sein. Der frühzeitige Beginn einer individualisierten - an einem festgelegten Ernährungsziel orientierten - klinischen Ernährungstherapie ist mit einer niedrigeren Mortalität von Intensivpatienten assoziiert. Der bevorzugte Applikationsweg ist enteral. Eine parenterale Ernährung als Ergänzung kann sinnvoll sein. Die klinische Ernährungstherapie orientiert sich an den aktuellen Leitlinien der Deutschen Gesellschaft für Ernährungsmedizin (DGEM). Die Ernährungstherapie beginnt mit einem Screening auf Mangelernährung, legt patientenindividuell Ernährungsziele fest und kontrolliert die Effektivität der Therapie in Bezug auf den aktuellen metabolischen Status, das Stadium der Erkrankung und dem Substratbedarf. Auf jeder Intensivstation soll ein Ernährungsstandard vorliegen. In diesem werden die o. g. Aspekte beschrieben. |
|
PICO |
Kann eine standardbasierte individualisierte klinische Ernährungstherapie im Vergleich zur rein mengenorientierten Therapie den Krankheitsverlauf und das patientenzentrierte Outcome positiv beeinflussen? |
|
Qualitätsziel |
Intensivpatienten erhalten eine standardbasierte, an den individuellen Bedarf angepasste Ernährungstherapie. Durch die Nutzung des Qualitätsindikators soll die Anzahl von Patienten die eine ungenügende Ernährungstherapie erhalten minimiert werden. |
|
Strukturqualität |
Ernährungsstandard vorhanden |
|
Prozessqualität Zähler 1 |
Anzahl der Patienten mit enteralem Ernährungsbeginn binnen 24 h |
|
Nenner 1 |
Anzahl aller Patienten, bei denen eine ausreichende orale Ernährung ab Tag 1 nicht absehbar war |
|
Zähler 2 |
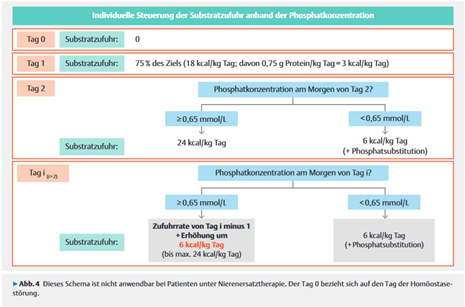
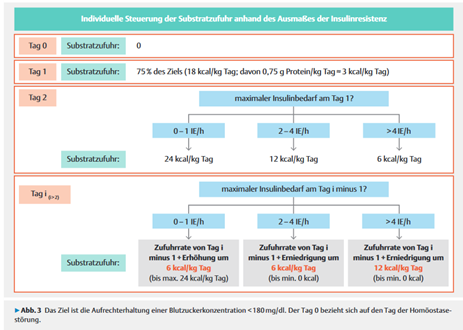
Anzahl der Patienten mit BMI ≤30, bei denen eine korrekte Ernährung anhand des berechneten Kalorienziels und eine Anpassung an den Metabolismus des Patienten erfolgte und dieses Ernährungsziel auch erreicht wurde |
|
Nenner 2 |
Anzahl aller klinisch ernährten Patienten mit BMI ≤30 |
|
Erklärung der Terminologie |
|
|
Datenquelle |
Abfrage Peer Review |
|
Richtwert |
|
|
Evidenzgrad |
Expertenkonsens |
|
QUALIFY |
fakultative Bewertung |
|
Beteiligte |
O. Kumpf, E. Muhl, A. Schäfer |
|
Interessenkonflikte |
Siehe Anlage |
|
Literatur |
(44, 45) |
|
Ergänzende Informationen |
Abb. aus: Elke G et al. Klinische Ernährung in der Intensivmedizin. Aktuel Ernährungsmed 2018; 43: 341–408
Abb. aus: Elke G et al. Klinische Ernährung in der Intensivmedizin. Aktuel Ernährungsmed 2018; 43: 341–408 |
Strukturierte Kommunikation mit Patienten und Angehörigen
|
Größenordnung |
Risiko und Effektivität |
|
Art des Indikators |
Prozess und Ergebnis |
|
Begründung |
Die intensivmedizinische Behandlung, ob elektiv oder als Notfall, muss mit dem Patientenwillen in Einklang stehen. Die Erwartungen und Ziele des Patienten müssen mit den Behandlungszielen der Intensivmedizin harmonieren. Es ist daher im Verlauf der intensivmedizinischen Behandlung zwingend notwendig, erreichte und geplante medizinische und pflegerische Behandlungserfolge mit dem Patientenwillen abzugleichen um möglichen Schaden vom Patienten, Angehörigen und den Behandelnden abzuwenden. Die Instrumente um diesen Abgleich zu erwirken, sind strukturierte Gespräche der behandelnden Mediziner, Pflegenden und Therapeuten mit der/m Patienten (und/oder) mit seinen/ihren Angehörigen bzw. mit bevollmächtigten Personen. Der Erfolg solcher Gespräche hängt ab von der Struktur des Gespräches und der qualifizierten Gesprächsführung der Intensivmediziner und Pflegekräfte. |
|
PICO |
Bei Angehörigen von Patienten auf einer Intensivstation führt eine strukturierte regelmäßige Angehörigenkommunikation und Dokumentation derselben zu einer Vermeidung von Belastungsstörungen und Depressionen bei diesen Angehörigen. Evidenzbasierte Kommunikationstechniken, die darauf fokussieren, gemeinsame Ziele der Gesprächspartner zu finden schützen sowohl Patienten, Angehörige und das Personal vor vermeidbaren Belastungen |
|
Qualitätsziel |
Verbesserung der Kommunikation mit Patienten und Angehörigen und Dokumentation von strukturierten Gesprächsinhalten. Vermeiden von PTSD, Depressionen und Ängsten bei Familienmitgliedern von Patienten. Vermeidung von ethischen Konflikten und interpersonellen Belastungen des Personals. |
|
Prozessqualität Zähler |
Erstes Gespräch durch FA / OA innerhalb von 72 Stunden nach Aufnahme inklusive schriftlicher Dokumentation (Richtwert 98%) und |
|
Nenner |
Alle Patienten der Intensivstation mit einer Liegedauer > 72 Stunden |
|
Ergebnisqualität |
Nutzung von Feedback-Plattformen zur Evaluation von Patienten- und Angehörigenzufriedenheit, z.B. Angehörigenbefragungen, Intensivtagebücher (Jährlicher Nachweis). |
|
Erklärung der Terminologie |
Die Kommunikation mit Patienten und Angehörigen auf der Intensivstation hat viele Formen. Die Verbindlichkeit von gemeinsamen Festlegungen kann nur durch strukturierte Gespräche und deren Dokumentation erreicht werden (Datum, Teilnehmer, Inhalte). Die Nutzung von Formblättern oder festen Masken im PDMS wird empfohlen. Zur Sicherstellung einer Versorgungskontinuität bei Therapiebeschränkungen sollten entsprechende Textvorlagen in der Krankenakte dokumentiert sein. Innerhalb von 72 Stunden nach der Übernahme auf die Intensivstation sollte ein Erstgespräch und in Folge mindestens einmal pro Woche ein Folgegespräch stattfinden. An den Gesprächen sollen der Patient bzw. dessen Angehörige/gesetzliche Vertreter, ein behandelnder Intensivmediziner, eine Pflegekraft und optional andere an der Behandlung beteiligte Fachärzte teilnehmen. Es soll ein formal strukturiertes Gespräch dokumentiert werden. Folgende Inhalte sollten dabei betrachtet werden:
Die Kommunikation soll darauf abzielen, die unterschiedlichen Informationsebenen zwischen Krankenhauspersonal und Patienten und deren Angehörigen insbesondere durch Unterstützung der Position von Patienten und Angehörigen auszugleichen (Empowerment patientenseitiger Gesprächsteilnehmer). Zu diesem Zwecke soll die Gesprächsführung aktuellen Empfehlungen folgen (VALUE-Konzept). Es wird empfohlen Patiententagebücher zur Unterstützung der Angehörigen zu verwenden. Hierbei ist auf die Vermeidung von Schuldgefühlen und Bekräftigung des Patientenwillens zu achten („was hätte er/sie jetzt gedacht und gesagt, wenn er/sie jetzt hier säße?“). Anzustreben ist eine partizipative Entscheidungsfindung (engl. shared decision making (SDM)). Die umfangreiche Information von Patientnen bzw. deren Angehörigen über verschiedene Behandlungsoptionen und deren Folgen ist hierbei als Voraussetzung zu sehen. Da stets verschiedene Handlungsoptionen bestehen, sind emotionale, kulturelle oder religiöse Bedürfnisse von Patienten und Angehörigen in den Entscheidungsprozess einzubinden. Intensivtagebücher: Das Intensivtagebuch stellt eine wirksame, evidenzbasierte Maßnahme zur Prävention von Angst und Depression nach einem Intensivaufenthalt bei Patienten und deren Angehörigen dar. Zudem unterstützen die täglichen Eintragungen in das Tagebuch Patienten nach dem Intensivaufenthalt beim Schließen von Erinnerungslücken. Fehlende bzw. irreale Erinnerungen werden wiederhergestellt bzw. richtig gestellt - der Gesundheits- bzw. Krankheitszustand wird visualisiert, Gedächtnislücken können besser geschlossen werden und die gesamte Situation des Aufenthaltes kann besser verstanden und nachvollzogen werden. Angehörigenbefragungen oder andere Möglichkeiten des Feedbacks können helfen, Defizite bei der Kommunikation zu entdecken. |
|
Datenquelle |
Abfrage, Peer Review |
|
Richtwert |
|
|
Evidenzgrad |
Expertenkonsens |
|
QUALIFY |
Fakultative Bewertung |
|
Beteiligte |
M. Brauchle, J.-P. Braun (Lead), A. Brinkmann, P. Czorlich, O. Kumpf, M. Ufelmann, R. Wildenauer |
|
Interessenkonflikte |
Siehe Anhang |
|
Literatur |
(7, 46-55) |
|
Ergänzende Informationen |
VALUE- Konzept: Value family statements: Würdigen, was die Angehörigen sagen; Wertschätzung Shared decision making (SDM): Seeking participation: Gesprächspartner suchen/animieren Intensivtagebücher: |
Frühmobilisation
|
Größenordnung |
Risiko und Effektivität |
|
Art des Indikators |
Prozess und Ergebnis |
|
Begründung |
Frühmobilisation, d.h. Mobilisation innerhalb von 72h nach Intensivaufnahme, ist ein energieverbrauchender Prozess mit dem Ziel, die Regenerationsfähigkeit der Muskulatur sowie die Funktionalität insbesondere Mobilität eines Patienten zu erhalten oder zu verbessern. Der Qualitätsindikator beinhaltet:
Ziele der Frühmobilisation sind eine verbesserte pulmonale Funktion, Erhaltung und Verbesserung der muskulären Regenerationsfähigkeit und Funktion, kardiovaskuläres Training, Unterstützung des Weaningprozesses, Alltags-Training, Förderung des psychosozialen Wohlbefindens, Re-Orientierung sowie Anregung der Vigilanz und Kognition mit dem Ziel der Vermeidung oder Verkürzung eines Delirs, verbesserte Kommunikation und Initiierung der Frührehabilitation. Weitere Ziele bestehen in der Vermeidung von Komplikationen wie Kontrakturen, Dekubitus, Pneumonien usw. Das Ergebnis sind eine signifikant kürzere Beatmungs- und Verweildauer auf der Intensivstation und gesteigerte funktionelle Unabhängigkeit bei Krankenhausentlassung. Die Effekte scheinen am besten, wenn a) protokollgestützt mobilisiert wird, und b) Patienten mit leichter-moderater Krankheitsschwere behandelt werden, wobei solche mit eingeschränktem Bewusstsein von Frühmobilisation profitieren. Die Dosierung (Frequenz, Dauer, Intensität) in Bezug auf spezielle Krankheitsbilder ist weiterhin unklar. Mögliche Formen der Frühmobilisation sind:
Unter Frühmobilisation wird die stufenweise Mobilisierung des Patienten innerhalb der ersten 72 Stunden nach Intensivaufnahme verstanden. Es wird empfohlen Maßnahmen zur Frühmobilisation in ein klinikinternes Behandlungskonzept zu integrieren und einen standardisierten Algorithmus hierfür zu erstellen, der dann jeweils patientenadaptiert umgesetzt wird. Zusätzlich wird empfohlen, eine medizinisch notwendige Immobilisierung immer explizit anzuordnen. |
|
PICO |
Haben kritisch erkrankte Patienten, deren Mobilisationsstart innerhalb von 72h nach Intensivaufnahme erfolgte, ein besseres funktionelles Outcome als Patienten, die nicht frühzeitig und strukturiert mobilisiert wurden? |
|
Qualitätsziel |
Sicherstellung ausreichender pflegerischer und physiotherapeutischer Ressourcen zur Durchführung von Frühmobilisation |
|
Prozessqualität Zähler |
Anzahl der Patienten bei denen Frühmobilisation stattgefunden hat |
|
Nenner |
Anzahl der Patienten, die auf Intensivstation aufgenommen wurden |
|
Ergebnisqualität Zähler |
Patiententage ohne Anordnung einer Nicht-Mobilisierung ohne medizinischen Grund |
|
Nenner |
Alle Patiententage |
|
Erklärung der Terminologie |
An der Frühmobilisation sind verschiedene Professionen beteiligt, u.a. Fachpflegende und Physiotherapeuten. Die Kriterien zur Frühmobilisation sollten lokal festgeschrieben werden. Hierbei können die in einer Consensus-Empfehlung publizierten Hinweise hilfreich sein, in der die Sicherheit von Mobilisationsmaßnahmen in Abhängigkeit von angewandten invasiven therapeutischen Verfahren beschrieben ist. |
|
Datenquelle |
Abfrage, Peer Review |
|
Richtwert |
|
|
Evidenzgrad |
Expertenkonsens |
|
QUALIFY |
Fakultative Bewertung |
|
Beteiligte |
R. Dubb, A. Kaltwasser, S.J. Schaller, P. Nydahl |
|
Interessenkonflikte |
Siehe Anhang |
|
Literatur |
(56-64) |
|
Ergänzende Informationen |
entfällt |
Personalbesetzung und Strukturvoraussetzungen einer Intensivstation
|
Größenordnung |
Eignung, Risiko und Effizienz |
||||||||
|
Art des Indikators |
Prozess |
||||||||
|
Begründung |
Dieser Qualitätsindikator fordert eine regelmäßige Selbstbewertung der qualitativen und quantitativen Vorgaben zur Personalbesetzung sowie der strukturellen Vorgaben gemäß den Empfehlungen der DIVI aus dem Jahr 2022 (X.1). Die Einhaltung der Strukturvorgaben soll einmal pro Jahr anhand einer Checkliste überprüft werden. Falls notwendig sollen Konsequenzen abgeleitet werden, die erreichbare Ziele beinhalten. Das Hauptaugenmerk liegt hierbei auf der Entwicklungsperspektive einer Intensivstation. |
||||||||
|
PICO |
Verbessert die jährliche Einschätzung des Erfüllungsgrades der Strukturempfehlungen der DIVI einer Intensivstation im Vergleich zu keiner Einschätzung. |
||||||||
|
Qualitätsziel |
Durch die Erfassung und Bewertung von Strukturkennzahlen anhand einer Checkliste werden potenzielle Defizite der personellen und strukturellen Ausstattung wahrgenommen und können zielgerichtet behoben werden. Ziel ist die adäquate Vorhaltung von speziell geschultem ärztlichen, pflegerischem und weiterem am Behandlungsprozess beteiligten Personal. Dadurch soll die optimale Behandlung von Intensivpatienten und die Vermeidung eines arbeitsbedingten Personalausfalls gewährleistet werden. |
||||||||
|
Strukturqualität Zähler |
Erreichte Punktzahl bei der Bewertung der Soll/Ist-Analyse der Strukturvorgaben anhand der Checkliste für die DIVI-Strukturempfehlungen. |
||||||||
|
Nenner |
Erreichbare Gesamtpunktzahl bei der Bewertung der Soll/Ist-Analyse der Strukturvorgaben anhand der Checkliste für die DIVI-Strukturempfehlungen. |
||||||||
|
Erklärung der Terminologie |
Die Checkliste zur Bewertung der Strukturvorgaben soll einmal jährlich z.B. im Rahmen einer internen Selbstbewertung bzw. eines DIVI-Peer Reviews ausgefüllt werden. Es wird empfohlen die Ergebnisse der Bewertung z.B. in einen PDCA-Zyklus einzubauen, mit dem der Umsetzungsgrad eingeleiteter Maßnahmen überprüft werden kann. Die Checkliste ist nach der folgenden Skala aufgebaut und orientiert sich an Erreichungsgraden für die jeweiligen Unterpunkte: Beschreibung der Skalenausprägung:
Ein Richtwert wird für den Indikator nicht festgelegt, um eine unerwünschte Nutzung zu vermeiden. Der erreichte Punktwert dient als Ausgangspunkt für einen kontinuierlichen Verbesserungsprozess (PDCA-Zyklus). |
||||||||
|
Datenquelle |
Checkliste, Interne Selbstbewertung, Peer Review |
||||||||
|
Richtwert |
Ohne Bewertung: Erreichte Punktzahl / Erreichbare Gesamtpunktzahl (Wert) |
||||||||
|
Evidenzgrad |
Expertenkonsens |
||||||||
|
QUALIFY |
|
||||||||
|
Beteiligte |
F. Bloos, A. Brinkmann, J.-P. Braun, P. Czorlich, C. Dame, R. Dubb, G. Gahn, E. Herting, A. Kaltwasser, O. Kumpf, G. Marx, A. Markewitz, E. Muhl, R. Riessen, M. Sasse, T. Schürholz, J. Weimann, R. Wildenauer, G. Wöbker, H. Wrigge |
||||||||
|
Interessenkonflikte |
Siehe Anhang |
||||||||
| Beteiligte | Alle Mitglieder der NSPR | ||||||||
|
Literatur |
(65) |
||||||||
|
Zusätzliche Informationen |
Checklisten zur Evaluation der Strukturempfehlungen der DIVI |